Kooperation: Wie sich Pflanzenpathogene mit anderen Schädlingen zu ihren Gunsten verbünden
Forschungsbericht (importiert) 2012 - MPI für Pflanzenzüchtungsforschung
Bedrohung der Welternährung durch Pflanzenschädlinge
Pflanzenkrankheiten bedrohen die Ernährung der Menschheit, da diese Krankheiten zu starken Ertragseinbußen oder gar zu kompletter Vernichtung der Erträge führen. Während Industrienationen durch hohe Ausgaben für Pflanzenschutzmittel Ertragsverluste begrenzen können, sind Entwicklungs- und Schwellenländer den Epidemien besonders durch neue Krankheitserreger ausgeliefert.
Trotz massiver Fortschritte in der Entwicklung von Pflanzenschutzmitteln und der Pflanzenzüchtung treten neue Krankheitserreger schneller auf als Schutzmaßnahmen entwickelt werden können. Ein Beispiel hierfür ist der Getreideschwarzrost. In Uganda wurde 1998 eine neue Variante dieses Rostpilzes entdeckt, die alle geläufigen Weizenrassen, auch diejenigen, die als nicht anfällig und daher resistent galten, infiziert. Der Pilz breitet sich inzwischen über den Iran weiter nach Osten aus und bedroht Indien und somit die Nahrungsgrundlage für Millionen Menschen [1]. Die ökologischen Grundlagen, die dazu führen, dass Pathogene, beginnend an Wild- oder Kulturpflanzen nachfolgend zu Epidemien an landwirtschaftlich relevanten Pflanzen führen, wurden bisher nur spärlich untersucht, obwohl gerade historische Beispiele deren Bedeutung aufzeigen. So konnte zum Beispiel durch Verringerung der Berberitzenbestände in den USA der Befall mit Schwarzrost deutlich reduziert werden, nachdem die Berberitze als wichtiger Zwischenwirt für die sexuelle Vermehrung des Pilzes identifiziert worden war [2]. Dieses und weitere Beispiele zeigen, wie wichtig es ist, ökologische Zusammenhänge zu verstehen, insbesondere die Biodiversität und Wechselwirkung von Organismen in ihren natürlichen Umgebungen, wenn man die Ernährung der immer noch zunehmenden Weltbevölkerung in Zukunft sichern will.
Entstehung der biotrophen Lebensweise von Pathogenen
Da Rostpilze sich nur auf lebenden Pflanzen entwickeln und vermehren können, haben sie im Laufe der Evolution ausgefeilte Methoden zur Besiedelung von Wirtspflanzen und zur Überwindung immer neuer Pflanzenschutzmaßnahmen errungen. Aufgrund der Abhängigkeit von einem lebenden Wirt werden diese Krankheitserreger als obligat biotroph (bios: leben, trophé: Ernährung) bezeichnet (Abb. 1).
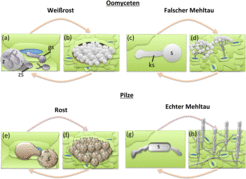
Lange war unklar, wie und und vor allem weshalb Pathogene sich derart an ihre Wirtspflanzen anpassen, dass sie ohne diese am Ende nicht mehr überleben können. Die vor kurzem erfolgte Sequenzierung und Analyse zahlreicher Genome biotropher Pathogene gab hierüber endlich Aufschluss. Es zeigte sich, dass alle Pathogene, die eine solche Lebensweise führen, zahlreiche Gene aus ihrem Genom verloren haben, die für wichtige Stoffwechselwege nötig sind, wie beispielsweise Gene für die Herstellung von Aminosäuren oder Vitaminen, aber auch Zellwand abbauende Enzyme, die wiederum bei denjenigen Pilzen vorhanden sind, die auf totem Pflanzenmaterial wachsen.

Da eine biotrophe Lebensweise nicht nur bei Pilzen, sondern auch bei anderen Organismen wie den mit Algen verwandten Oomyceten auftritt, war es interessant, Vergleiche von Genomen filamentös wachsender Schädlinge ganz unabhängig von ihrem Verwandtschaftsgrad durchzuführen. Die Auswertung des Genoms des falschen Mehltaus [3] sowie des Weißrosterregers [4] (Abb. 2) zeigten ebenfalls einen Verlust zahlreicher für den Stoffwechsel wichtiger Gene und bestätigen damit, dass es sich möglicherweise um einen bei allen biotrophen Pflanzenpathogenen vorkommenden Mechanismus handelt.
Weshalb aber verliert ein Organismus wichtige Gene aus seinem Genom? Schon vor 150 Jahren entdeckte deBary [5], dass Pflanzenpathogene, insbesondere solche mit biotrophem Lebensstil, Strukturen entwickeln, die in die pflanzliche Zelle hineinreichen. Diese hoch spezialisierten Strukturen wurden Haustorien (haurire: herausschöpfen) genannt (Abb. 3) und es stellt sich heraus, dass sie wahrscheinlich den Pathogenen zur Aufnahme von Nährstoffen dienen. Wie solche Strukturen jedoch in der pflanzlichen Zelle gebildet werden können, ohne dass sie abstirbt oder diese Attacke wirksam bekämpft, blieb lange unklar. Erst die Sequenzierung zahlreicher Genome und experimentell ermittelte Daten zeigten, dass biotrophe Pathogene ein ausgeprägtes Repertoire an Proteinen besitzen, die in der Lage sind, die Abwehr der Pflanze zu unterdrücken. Es wurde daher die Hypothese aufgestellt, dass dieses komplexe Repertoire an Proteinen auch die Differenzierung von Strukturen zur Aufnahme von Nährstoffen ermöglicht. Denn: Die Nährstoffaufnahme aus einer lebenden Wirtszelle bedingt, dass Substanzen, für deren Erzeugung viel Energie benötigt wird und somit das Wachstum des Pathogens limitieren kann, nicht mehr hergestellt werden müssen. Gene, die für die Herstellung dieser Nährstoffe unabdingbar waren, wurden nunmehr nicht mehr benötigt und gingen daher über die Generationen hinweg verloren mit der Folge, dass das Pathogen sich spezifisch an seinen Wirt gebunden hat [6].
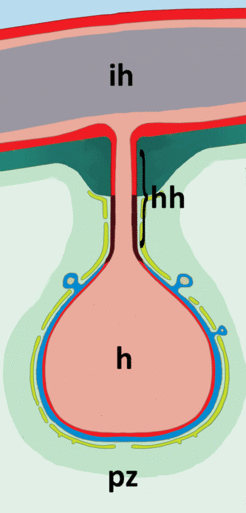
Abb. 3: Haustorien (h) sind differenzierte Strukturen von Pilzen oder Oomyceten, die die Pathogene in die lebende Wirtszelle (pz) einsenken, um Nährstoffe zu mobilisieren und gleichzeitig Moleküle in die Zelle abzugeben, um deren Immunabwehr zu unterdrücken und dennoch die Zelle am Leben zu erhalten. Die Haustorien bleiben über eine Art Hals (hh) mit dem pathogenen Organismus verbunden, sodass die pflanzlichen Nährstoffe über die Infektionshyphe (ih) bis in die Sporen transportiert werden können.
Kompromiss für sexuelle Rekombination
Wirt–Pathogen Wechselwirkungen wurden bisher im Wesentlichen auf die Interaktion von zwei Organismen miteinander reduziert. Zunehmend wird jedoch klar, dass dieses reduktionistische Bild nur begrenzt umgesetzt werden kann, da in natürlichen Umgebungen vielfältige Wechselwirkungen mit anderen Organismen möglich sind [7, 8]. Um die Entstehung neuer Krankheiten zu erklären, ist es daher wichtig, den ökologischen Kontext, insbesondere deren Wechselspiel mit anderen Organismen, zu verstehen.
Bereits in den 1950er-Jahren wurde beschrieben, dass Rostpilze in der Lage sind, die Immunabwehr ihrer Wirtspflanze so weit zu unterdrücken, dass Viren, die sonst nicht diese Pflanze befallen, nach Rostinfektion in der Lage sind, sich auszubreiten. Vergleichbares wurde auch für Erstinfektionen mit echten Mehltaupilzen beobachtet. Hier zeigte sich sogar, dass sie die Abwehr so weit unterdrücken, dass andere echte Mehltaupilze, die üblicherweise von der Immunabwehr der Pflanze erkannt und getötet werden, diese nun infizieren und sich vermehren konnten. Da dies nicht nur bei biotrophen Pilzen der Fall ist, sondern auch bei biotrophen Oomyceten, muss es sich um ein generelles Merkmal dieser Lebensweise handeln (Abb. 4). Trotz ihrer von Pilzen sehr verschiedenen Abstammung zeigen Oomyceten vergleichbare Infektionsstrategien, sowohl was die Ausbildung von Haustorien als auch die Bildung von Vermehrungsstrukturen wie Sporen angeht [6]. Insbesondere für den häufig an Kultur- und Wildpflanzen auftretenden Weiß-Rost konnte eine sehr effiziente Unterdrückung der pflanzlichen Immunabwehr nachgewiesen werden. In der Natur tritt Weiß-Rost daher oft zusammen mit anderen Oomyceten und Pilzen auf. Untersuchungen zeigten zudem, dass Weiß-Roste außerdem noch das Wachstum von Bakterien auf der befallenen Pflanze begünstigen.

Eine zwingende Frage, die sich hieraus ergibt, ist: Warum unterdrücken biotrophe Pathogene die pflanzliche Abwehr so weit, dass weitere Pathogene und sogar Nicht-Pathogene wie Hefen oder andere, nicht angepasste Pathogene in der Lage sind, auf demselben Wirt zu wachsen und somit mit dem erstinfizierenden Pathogen um Ressourcen zu konkurrieren?
Eine Erklärung könnte mangelnder genetischer Austausch sein, da die biotrophe Lebensweise nicht nur eine zwingende Bindung an lebende Pflanzen mit sich bringt, sondern aufgrund dieser komplexen Wechselwirkungen nur eine bestimmte Pflanzenart von einem bestimmten Pathogen infiziert werden kann. Um dennoch neue Lebensräume zu besiedeln oder neu auftretende Abwehrmechanismen der Wirtspflanze zu überwinden und sich anzupassen, benötigen Pathogene innerhalb ihrer Art möglichst viele individuelle und verschiedene Variationen ihrer für die Infektion wichtigen Gene. Um diesen Gen-Pool zu „befüllen“, ist ein sexueller Austausch zwischen verschiedenen Pathogen-Varianten nötig. Da aber biotrophe Pathogene sehr spezialisierte Wirtskreise haben, ist ein zufälliger Austausch auf derselben Pflanze nahezu unmöglich. Es wird daher angenommen, dass die Unterdrückung der Abwehr dazu dienen könnte, potenziellen Kreuzungspartnern, die nicht an denselben Wirt angepasst sind, ein Wachstum auf der befallenen Wirtspflanze zu ermöglichen. Durch Sequenzierung mehrerer Genome des Weißrosterregers von Broccoli, Gartenschaumkraut und Ackerschmalwand (vgl. Abb. 2) konnte gezeigt werden, dass trotz nicht überlappender Wirtspflanzen sexuelle Rekombination zwischen den Isolaten erfolgte. Effektive Unterdrückung der Abwehr scheint daher bei biotrophen Pathogenen für eine Aufrechterhaltung der Art unentbehrlich zu sein.
Zu einer Wirt–Pathogen Interaktion gehören immer zwei, oder noch mehr?
Es wurde beobachtet, dass es auf mit biotrophen Pathogenen befallenen Pflanzen zu einer massiven Vermehrung von Bakterien kommen kann. Warum verhindern obligat biotrophe Pathogene nicht das Wachstum von Bakterien, zumal doch besonders Pilze bekanntermaßen dazu in der Lage sind, Antibiotika für genau diesen Zweck zu produzieren und so die Konkurrenz von Bakterien zu reduzieren? Um diese Frage zu beantworten, muss zunächst verstanden werden, wie viele und welche Bakterienarten spezifisch mit biotrophen Pathogenen interagieren, was im Moment Gegenstand der Forschung ist. Es konnte kürzlich gezeigt werden, dass im Laufe der Evolution zahlreiche Gene von Bakterien in das Genom von Pilzen, insbesondere Oomyceten, übertragen wurden [9]. Man spricht in diesem Fall von horizontalem Gentransfer, da Gene zwischen verschiedenen Arten beziehungsweise Lebensformen, die nicht sexuell kompatibel sind, übertragen werden. Einen Transfer von Genen, der durch sexuellen Austausch von Generation zu Generation erfolgt, bezeichnet man als vertikal. Für viele Oomyceten zeigte sich, dass horizontaler Gentransfer für die Weitergabe der zahlreichen Gene verantwortlich ist, die für die Besiedlung von Wirtspflanzen eine Rolle spielen. Es ist daher ein großes Anliegen, weitere Genome verschiedener bakterienassoziierter Isolate zu sequenzieren, um den Ursprung dieser Gene zu ermitteln. Für die Erfassung der Genome von Pathogenen und ihrer assoziierten Organismen wird eine Methode verwendet, die als Metagenomics bezeichnet wird. Hierfür werden infizierte Pflanzen an Feld- und Wegrändern zusammen mit infizierten Kulturpflanzen gesammelt und dank moderner, schneller und preisgünstiger Sequenzierungsmethoden vollständig sequenziert. Durch speziell dafür entwickelter Computeranalysen können die zunächst im Gemisch sequenzierten Genome getrennt und analysiert werden, um nachfolgend Aussagen über diejenigen Gene in der Lebensgemeinschaft aus Pflanze, Pilzen, Oomyceten und Bakterien zu ermöglichen, die die Entwicklung eines gegebenen Pathogens fördern oder initiieren. Die Isolierung der an der Gemeinschaft beteiligten Organismen und eine Schritt für Schritt Rekonstruktion dieser einst natürlich entstandenen Gemeinschaft im Labor wird neue Erkenntnisse darüber bringen, wie neue Pathogene entstehen und wie das ökologische Umfeld, insbesondere die am Ort vorhandene Biodiversität, dazu beiträgt.



