Anwendung von activity-based proteomics zur Analyse von Pflanzen-Pathogen Interaktionen
Forschungsbericht (importiert) 2006 - MPI für Pflanzenzüchtungsforschung
Protein-Profilierung
Unter Proteinprofilierung versteht man die Bestimmung der relativen Häufigkeit von Proteinen eines untersuchten Organismus. Mit den Methoden der Proteinprofilierung ist es in der heutigen post Genom-Ära möglich, eine enorme Fülle an Informationen über Genome, Transkriptome und Proteome lebender Organismen zu erhalten und damit verschiedene biologische Prozesse zu beschreiben. Die tatsächliche Aktivität der Proteine/Enzyme lässt sich jedoch nicht ohne weiteres aus ihrer Präsenz ableiten, da sie überwiegend durch post-translationale Prozesse wie Phosphorylierung, Translokation oder durch Prozessierung reguliert wird. Technologien, die in der Lage sind, die Aktivität von Proteinen zu beschreiben, wie zum Beispiel das activity-based profiling, sind deshalb von entscheidender Bedeutung für das tiefergehende Verständnis biologischer Prozesse.
Was versteht man unter activity-based profiling?
Activity-based profiling ist eine Technik, mit der man die Aktivität einzelner Proteinklassen bestimmen kann. Dazu werden Zellextrakte mit spezifischen, biotinylierten (oder anderweitig markierten) Inhibitoren inkubiert, die ausschließlich mit aktiven Zielmolekülen reagieren können (Abb. 1) [1].
Es entsteht eine kovalente, irreversible Bindung zwischen Enzym und markiertem Inhibitor, die die nachfolgende Analyse unter denaturierenden Bedingungen erlaubt (Abb. 1A). Markierte Proteine können gereinigt und auf Proteinblots detektiert werden. Ihre Identität lässt sich durch Massenspektrometrie bestimmen. DCG-04 ist ein Paradebeispiel einer auf Aktivität basierenden Sonde (Abb. 1B) und wurde erfolgreich eingesetzt, um die Aktivität von papainähnlichen Cysteinproteasen in Pflanzen zu untersuchen (Abb. 1C) [2].
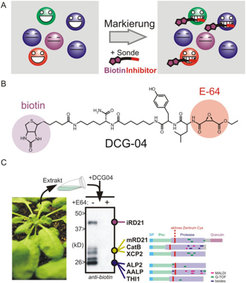
Die auf Aktivität basierenden Sonden bestehen aus drei Untereinheiten: einem Inhibitor, einem Abstandshalter und einem Reporter. Die Inhibitoreinheit leitet sich in den meisten Fällen von spezifischen irreversiblen Inhibitoren ab (im Fall von DCG-04 ist dies E-64). Sie kann aber auch eine reversibel bindende Einheit sein, die mit einer photoreaktiven Gruppe verknüpft ist. Die kovalente Verknüpfung des Inhibitors mit dem Protein (zum Beispiel Metalloprotease) erfolgt dann über eine lichtinduzierte Reaktion. Der Abstandshalter schließlich verbindet die Inhibitor- mit der Reportereinheit. Er erhöht so die Spezifität der Sonde und beeinflusst ihre Löslichkeit. Die Reportereinheit wird für die spätere Analyse beziehungsweise Isolierung der markierten Proteine benötigt. Die Art der Reportereinheit bestimmt wiederum, welche Methode zur Reinigung und Detektion der markierten Proteine verwendet werden muss.
Untersuchung „aktiver“ Enzymklassen
Aktivitätssonden wurden bereits für viele verschiedene Enzymklassen, insbesondere jedoch für hydrolytische Enzyme, wie beispielsweise Proteasen, beschrieben [1]. Proteasen katalysieren die Hydrolyse von Peptidbindungen in Proteinen und können, je nach ihrer evolutionären Abstammung, in unterschiedliche Klane eingeordnet werden. Sonden für papainähnliche Cysteinproteasen (Klan CA), caspaseartige Enzyme (Klan CD) und Proteasom- und ubiquitinartige Proteasen (Klan CE) wurden bereits entwickelt. Weiterhin sind Photoaffinitätssonden beschrieben worden, mit denen die Aktivität von Metallo- und Aspartatproteasen untersucht werden kann. Darüber hinaus gibt es außerdem eine ganze Reihe von Sonden für die Analyse von Kinasen, Phosphatasen, Glycosidasen und Serinhydrolasen.
Die Markierung der Aktivität von Proteasen in vivo ist den in vitro-Ansätzen überlegen, da sie direkt in noch lebenden und intakten Zellen durchgeführt wird. Biotinylierte Sonden sind üblicherweise jedoch nicht membranpermeabel, was ihre Anwendbarkeit in vivo stark einschränkt. Eine Möglichkeit für die Analyse von Proteinaktivitäten in lebenden Zellen ist zum Beispiel der Einsatz permeabler, fluoreszierender Sonden, die die subzelluläre Lokalisation von Enzymaktivitäten detektieren können. Eine verfeinerte Version dieser Sonden ist sogar mit einem intramolekularen Fluoreszenzlöscher verknüpft, der die Fluoreszenz ungebundener Sonden unterbindet. Erst durch die Reaktion mit einer Protease wird der Fluoreszenzlöscher entfernt und die Fluoreszenz wiederhergestellt. Dieser Kunstgriff garantiert, dass das detektierte Fluoreszenzsignal nur durch die Aktivität eines Enzyms hervorgerufen wird. Ein anderer Ansatz, mit dem die in vivo-Aktivität von Enzymen abgebildet werden kann, macht sich das Konzept der „Click-Chemie“ zunutze. Hier werden Proteine lebender Zellen zuerst mit einem membranpermeablen, chemisch modifizierten Inhibitor markiert, dann extrahiert und in vitro unter kontrollierten Bedingungen mit einem Reporter versehen. Auch diese Methode konnte für Untersuchungen an Pflanzen erfolgreich adaptiert werden. Sie erlaubt es, nicht nur die Aktivität von Proteinen in vivo abzubilden, sondern vereinfacht auch die Synthese von neuen Sonden.
Welche biologischen Prozesse können untersucht werden?
Prinzipiell kann jeder biologische Prozess mittels activity-based profiling untersucht werden. Die Wissenschaftler der Plant-Chemetics-Gruppe wollen genauer verstehen, wie das Pathogen Pseudomonas syringae Pflanzen der Art Arabidopsis thaliana infiziert. Während nämlich die Wechselwirkung dieser zwei Organismen auf genetischer Ebene bereits sehr gut verstanden ist, sind Informationen über Enzymaktivitäten spärlich. Die Prozesse, die es einem Pathogen ermöglichen, seine Wirtspflanze zu kolonisieren, sind faszinierend. Um die Abwehrreaktionen der Pflanze zu unterbinden und Nährstoffe zu mobilisieren, programmiert das Pathogen zum Beispiel den Meta- und Katabolismus der Pflanzenzelle um. Dieser Aspekt der Forschung an der Wirt-Pathogen Interaktion blieb bisher weitgehend unbeachtet, da sich die meisten Forschungsprojekte der Genetik und Molekularbiologie der pflanzlichen Immunität widmeten. Eine ganze Reihe von Indizien spricht dafür, dass Proteasen bei der Wechselwirkung zwischen Mikroben und Pflanzen eine wichtige Rolle spielen (Abb. 2) [3-5], aber viele Fragen sind noch offen.
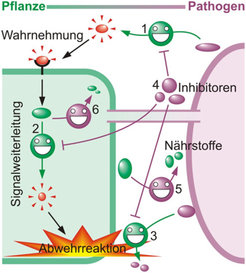
Enzyme, die eine veränderte Aktivität während der Infektion von Arabidopsis durch Pseudomonas zeigen, werden genau untersucht, um ihre Rolle bei der Pflanze-Pathogen-Wechselwirkung besser zu verstehen. Verschiedene Untersuchungsmethoden kommen dabei zur Anwendung. Der traditionellen reversen Genetik folgend, werden Arabidopsis knock-out- und Überexpressionslinien mit Pathogenen infiziert und die Unterschiede in den auftretenden Phänotypen bewertet. Diese Pathogen-Assays können auch in Nicotiana benthamiana Blättern erfolgen, in denen das Transkriptionsniveau endogener Enzyme durch Virus-induzierte Gen-Inaktivierung (virus-induced gene silencing, VIGS) reduziert wurde. Außerdem wird zielgerichtete chemisch-reverse Genetik angewendet, um die Funktion eines aktiven Enzyms zu bestimmen [6]. Hierbei wird eine von bekannten Inhibitoren abgeleitete Chemikalien-Bibliothek durchmustert und nach Korrelationen zwischen i.) einem von der Chemikalie verursachtem Phänotyp und ii.) der Hemmung einer Enzymaktivität gesucht: Letztere kann durch activity-based profiling verfolgt werden. Diese Herangehensweise ist sehr schnell und umgeht gleich mehrere Probleme der traditionellen reversen Genetik, wie zum Beispiel Redundanz und Sterblichkeit.
Die Wissenschaftler des Max-Planck-Instituts für Züchtungsforschung hoffen nicht nur, dass diese interdisziplinäre Forschung nützliche chemische Werkzeuge schafft, um biologische Fragestellungen aus völlig neuen Blickwinkeln zu beleuchten, sondern sie sind auch zuversichtlich, dass die intensive Zusammenarbeit zwischen Biologen und Chemikern das generelle Potenzial fachübergreifender Forschung verdeutlicht.

